前言 人要活著就需要有支撐活著所需要的營養素,在目前醫學已知的醫學裡,人類所需的營養素有蛋白質、碳水化合物、脂質、礦物質、維生素和最近幾年所重視的植化素等六大類。從本輯起將陸續做簡明扼要的介紹。
認識蛋白質與胺基酸
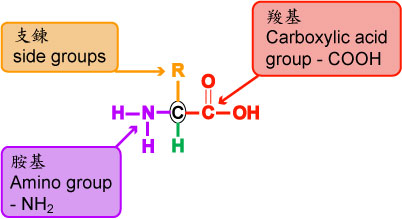
蛋白質的結構
構成蛋白質的主要成分有碳、氫、氧和氮元素,有的也含磷、鐵、銅等。其中氮的含量約有16%左右,所以分析蛋白質含量時,常以氮的含量乘以6.25倍即粗蛋白質的含量。
蛋白質的理化特性與酸鹼性 :
蛋白質的功能
蛋白質在體內扮演極為重要的功能,舉凡生命的功能,蛋白質都有參一腳。主要功能簡述如下:
1. 是細胞的主成分
2. 是肌肉的主成分
3. 酵素作用
4. 荷爾蒙的作用
5. 具有運送功能之蛋白質:例如血紅素、脂蛋白等。
6. 形成抗體,扮演免疫功能。
7. 平衡水份
8. 電解質的平衡功用
9. 酸鹼平衡的功用
10. 提供熱量
胺基酸的分類
胺基酸可分為必需胺基酸、半必需胺基酸和非必需胺基酸等三類。人體內不能自行合成而必須仰賴食物直接供應的稱為必需胺基酸,成人需要9種,嬰孩需要10種﹙加上精安酸﹚;有些胺基酸在特殊狀況下體內需要量特別多,或是體內合成能力不足,必須由飲食中攝取補充的稱為半必需胺基酸;身體能夠自行合成足夠量的稱為非必需胺基酸。
必需胺基酸(9種) :色胺酸(Trp)、纈胺酸(Val)、異白胺酸(Ile)、羥丁胺酸(Thr)、離胺酸(Lys)、苯丙胺酸(Phe)、白胺酸(Leu)、甲硫胺酸(Met)、組胺酸(His)
半必需胺基酸 :
醯胺麩胺酸﹙Gln﹚: 手術、外傷病人。
非必需胺基酸 :甘胺酸(Gly)、麩胺酸(Glu)、酪胺酸(Tyr)、丙胺酸(Ala)、絲胺酸(Ser)、半胱胺酸(Cys)、胱胺酸(Cyn)、脯胺酸(Pro)、氫氧基脯胺酸、天門冬酸(Asp)、瓜胺酸(Cit)、氫氧基麩胺酸。
補充說明
1. 必需胺基酸 是指只存在食物中,動物無法合成,只能由食物中攝取,則這些 胺基酸 被稱為必需胺基酸。動物需攝取必需胺基酸以製造 蛋白質 。由於不同物種的化合能力不同,對於某一物種是必需胺基酸的,對另一物種則不一定是必需胺基酸。
2. 胺基酸的互換:有些胺基酸可以用必需胺基酸為原料而代謝生成。
蛋白質的消化與吸收
蛋白質的主要功用在於供應人體所需的各種胺基酸,因此來自各種動植物食品的蛋白質都必須分解成胺基酸,才能供人體利用。
胺基酸的代謝與利用
1.合成作用: 合成人體所需的各樣蛋白質
2.生成葡萄糖: 在醣類供應不足時,肝與腎可利用胺基酸來合成葡萄糖以維持血糖濃度
3.生成脂肪: 過量胺基酸在肝中轉換成脂肪,可運送至脂肪組織儲存
4.供應熱量: 每公克提供 4 大卡
5.代謝廢物: 胺基酸代謝為能量或生成葡萄糖與脂肪酸時,分子中的氮在肝臟代謝為尿素,由腎臟排泄。由尿液中之氮含量,可推測體內蛋白質的耗損狀況。
蛋白質的合成原則與應用
細胞進行蛋白質合成反應時,遵循全或無定律,作為原料的胺基酸種類和含量都必須齊全。胺基酸從食物或體內蛋白質分解而來,如果任一種必需胺基酸不足,合成反應就會中止。
從氮平衡的觀念看蛋白質的需要量
由於氮是蛋白質特有的元素,因此追蹤氮的攝取和排泄可以反應蛋白質的利用狀況。因此蛋白質的平衡以氮平衡來代表,其公式表示如下:
氮平衡 =食物攝食之氮 - 排泄之氮 (糞便、尿、汗、皮膚、毛髮…)
氮平衡可分為三種狀態:正、平衡、負。健康的成年人應該維持氮平衡。成長中的嬰幼兒、兒童、青少年、懷孕的婦女、病後調養復原時,都應維持正氮平衡。任何情況下,負氮平衡均有損健康。以氮平衡為標準可以估計人體對必需胺基酸與蛋白質的需要量。蛋白質的品質 限制胺基酸 :互補原則 :補充說明 :健康靈性的蛋白質來源 http://minibaba.pixnet.net/blog/category/85506 。攝取原則 :儘管某些食物所含的蛋白質和胺基酸超高,但是在攝取上仍應以多樣性較好,例如選用多種不同的豆類和穀物時常搭配。況且植物內尚有多種營養素未被發現,所以還是要重視均衡與多樣性。蛋白質缺乏症
附加說明
1. 蛋白質由胺基酸構成,每個蛋白質都有特定的胺基酸種類以及排列的次序,並且形成獨特的立體形狀。結構正常才有正常的生理活性與功能,加熱或酸鹼處理會破壞結構,使蛋白質喪失作用。
2. 食物中的蛋白質有時會引起過敏反應 。
繼續閱讀
蛋白質的四級結構
一級結構 (primary structure)
組成蛋白質多肽鏈的線性胺基酸序列。
二級結構 (secondary structure)
依靠不同胺基酸之間的 C=O 和 N-H 基團間的 氫鍵 形成的穩定結構,主要為α螺旋和β摺疊。 加熱或酸鹼條件下會破壞此種結構,稱為蛋白質變性。
三級結構 (tertiary structure)
通過多個二級結構元素在三維空間的排列所形成的一個蛋白質分子的三維結構,是單個蛋白質分子的整體形狀。蛋白質的三級結構大都有一個疏水核心來穩定結構,同時具有穩定作用的還有鹽橋、氫鍵和二硫鍵等。常常可以用「摺疊」一詞來表示「三級結構」。例如血紅素,或是纖維狀蛋白質如膠原蛋白。
四級結構 (quaternary structure)
用於描述由不同多肽鏈( 亞基 )間相互作用形成具有功能的蛋白質複合物分子的形態。 由多條胜鏈拼合而成,例如血紅素含有 4 條胜鏈。
遺傳性疾病 蛋白質的構型 蛋白質組 蛋白質的大小 蛋白質的發現史
minibaba 發表在 痞客邦 留言 (0) 人氣(


 留言列表
留言列表


 {{ article.title }}
{{ article.title }}